OECD TG-407囓齒類動物的28天重複劑量 吞食毒性研究
OECD TG-407 Repeated Dose 28-day Oral Toxicity Study in Rodents
毒理試驗(OECD GLP實驗)
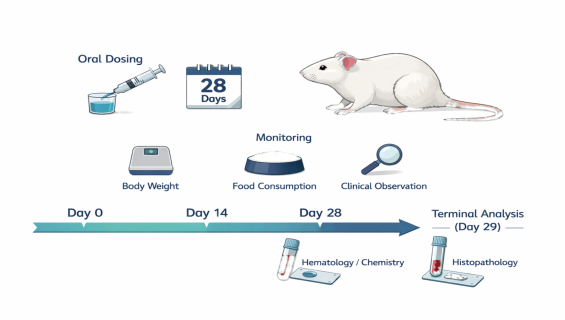
OECD TG 407:囓齒類動物 28 天重複劑量吞食毒性研究
在化學物質或藥物開發的中期階段,了解長期攝取對生理機能的累積性影響至關重要。我們遵循 OECD TG 407 標準與 GLP 規範,透過為期 28 天的連續給藥觀察,為您的產品提供關鍵的亞慢性毒性數據,協助判定安全攝取量。
試驗目的
評估受試物質經口重複給藥 28 天後,對囓齒類動物(通常為大鼠)所產生的毒性特徵。主要用於判定目標器官、觀察劑量效應關係,並估算無可見不良反應劑量 (NOAEL)。
服務特色與技術指標
-
精準給藥模式: 提供餵飼 (Dietary)、飲水 (Drinking water) 或胃灌食 (Gavage) 等多種給藥方式。
-
全方位生理檢測:
-
臨床觀察: 每日監測行為、皮膚、毛髮及神經系統表現。
-
血液與生化分析: 評估肝腎功能、代謝指標及造血系統影響。
-
功能性觀察 (FOB): 包含感覺反應、抓地力及運動協調能力測試。
-
-
病理學鑑定: 試驗結束後進行大體解剖、器官重量測量及組織病理學切片檢查。
-
恢復組設置: 視需求設置恢復組,觀察停藥後毒性反應是否具有可逆性。
試驗流程簡介
-
劑量設定: 設置高、中、低三個劑量組及一空白對照組。
-
連續暴露: 每日定時定量給藥,持續 28 天。
-
定期監測: 每週記錄體重、攝食量,並進行臨床症狀掃描。
-
最終評估: 採集血樣、尿樣並進行病理切片分析。
-
報告產出: 提供符合國際申報標準的完整 GLP 毒理數據報告。
適用領域
-
新化學物質申報與登記 (REACH / TSCA)
-
食品添加物與營養成分安全評估
-
藥物開發臨床前安全性試驗
-
農藥與環境用藥亞慢性毒性鑑定
付款方式請點我