OECD TG-422 結合重複劑量毒性研究與生殖/發育毒性篩選試驗
OECD TG-422 Combined Repeated Dose Toxicity Study with the Reproduction/Developmental Toxicity Screening Test
毒理試驗(OECD GLP實驗)
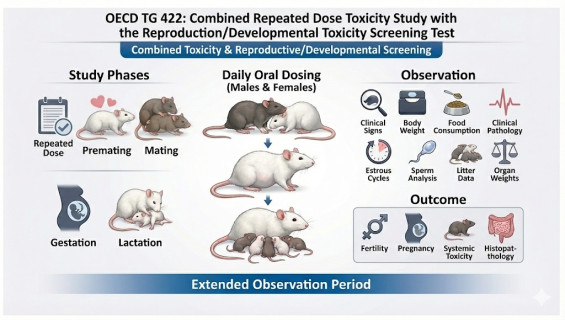
OECD TG 422:結合重複劑量毒性與生殖/發育毒性篩選試驗
在追求法規合規與時間效率的平衡時,OECD TG 422 提供了一個極具優勢的解決方案。我們遵循 GLP 規範,將「重複劑量毒性」與「生殖發育篩選」結合於單一研究中,旨在減少實驗動物使用量,同時為您的產品提供全方位的毒理輪廓。
試驗目的
本試驗旨在同步評估受試物質在重複暴露下的全身性毒性(目標器官影響)以及對生殖功能(雄性與雌性生育力)與子代早期發育的潛在風險。
服務特色與技術指標
-
高資訊整合度: 單一試驗即可獲得重複劑量毒性、神經毒性篩選、生殖毒性及發育毒性等多項數據。
-
全身性毒性評估: 包含詳細的臨床觀察、體重攝食量追蹤、血液學與臨床生化分析。
-
生殖與發育篩選: 監測親代交配表現、受孕率、分娩狀況及子代出生後的存活與發育情形。
-
功能性觀察 (FOB): 納入感覺反應與運動活動測試,初步評估受試物質的神經毒性潛力。
-
符合經濟效益: 有效整合資源,是 REACH 法規附件 VIII (10-100 噸/年) 的核心要求。
試驗流程簡介
-
親代暴露: 雄性給藥至少 28 天;雌性自交配前 2 週開始給藥,持續至分娩後第 13 天。
-
臨床與功能性檢查: 於給藥期間進行臨床症狀掃描及功能性觀察測試(FOB)。
-
生殖階段: 紀錄交配、受孕、分娩及授乳期的各項指標。
-
終點評估: 進行血液、尿液分析,並對親代器官與子代進行完整的大體解剖與組織病理學鑑定。
適用領域
-
化學物質法規申報 (REACH Annex VIII)
-
產品開發早期的綜合風險評估
-
農藥與工業化學品的初步毒性特徵鑑定
-
需快速取得多維度毒理數據的研發專案
付款方式請點我