OECD TG-471 細菌回復突變試驗/致變異性試驗
OECD TG-471 Bacterial Reverse Mutation Test
毒理試驗(OECD GLP實驗)
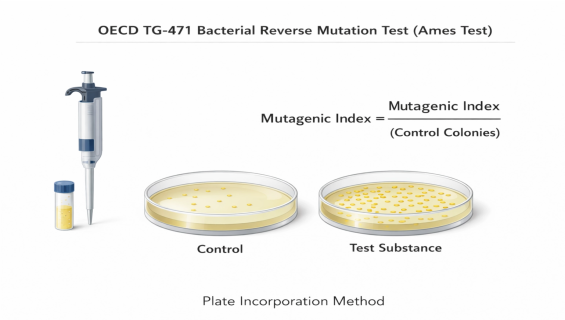
細菌回復突變試驗的科學解密
OECD 測試指南 471(Test Guideline 471),通常被視為化學品安全評估中的基石之一,其正式名稱為「細菌回復突變試驗」(Bacterial Reverse Mutation Test)。這項試驗的目標是作為一種初步篩選工具,用於快速且經濟地評估化學物質是否具有引起基因毒性(Genotoxic Activity)的潛在能力。
1. 檢測核心:危險的「點突變」
基因毒性的危害主要來自於對遺傳物質(DNA)的永久性損害。TG 471 實驗的核心在於檢測一種稱為「點突變」(Point Mutations)的特定 DNA 損傷。點突變是指 DNA 序列中,單一或少數幾個鹼基對發生替換、添加或刪除的微小變化。雖然這種變化看似微不足道,但資料指出,點突變與許多人類遺傳性疾病以及體細胞中癌基因和腫瘤抑制基因的腫瘤形成過程密切相關。
TG 471 正是透過偵測兩種主要類型的點突變來評估化學品的潛在危害:
- 鹼基替換突變(Base Substitution Mutagens):改變 DNA 中的鹼基對,。
- 移碼突變(Frameshift Mutagens):導致 DNA 中添加或刪除一個或多個鹼基對,改變了遺傳密碼的「閱讀框架」。
2. 實驗原理:讓「殘缺」的細菌起死回生。
這項試驗之所以被稱為「回復突變」(Reverse Mutation),是因為它的機制是建立在修復一個預先存在的缺陷之上。
實驗室使用的模型: TG 471 試驗使用經過特殊設計的沙門氏菌(Salmonella typhimurium)和大腸桿菌(Escherichia coli)菌株。這些菌株被稱為「營養缺陷型」,因為它們被賦予了無法合成某種生長必需氨基酸(例如組氨酸或色氨酸)的基因缺陷。
回復突變的過程:
1. 將這些殘缺的細菌懸浮液暴露於待測化學物質中。
2. 如果該化學物質具有致突變性,它會對細菌的 DNA 造成進一步的突變。
3. 如果這個新的突變剛好逆轉了(revert)原有的缺陷,那麼細菌就重新獲得了合成該必需氨基酸的能力。
4. 隨後,研究人員將混合物塗布在一個缺乏該必需氨基酸的培養基上。
5. 在兩到三天 (48 至 72 小時) 的孵育後,只有那些發生了「回復突變」、重新獲得生長能力的細菌才能形成菌落。
6. 計數這些「突變菌落」(revertant colonies)的數量,並將其與未暴露於化學物質的溶劑對照組(solvent control)的自發突變菌落數進行比較,即可判斷化學物質是否具有致突變性。
為了確保對各種致突變機制都能有效檢測,試驗必須使用至少五種菌株。例如,許多沙門氏菌菌株的突變位點是 GC 鹼基對,因此可能無法檢測某些氧化性誘變劑;因此,建議加入 AT 鹼基對突變位點的菌株,如大腸桿菌 WP2 菌株或沙門氏菌 TA102。
3. S9 混合物的必要性:模擬人體代謝
在評估化學物質毒性時,最大的挑戰之一是:許多物質本身無害,但被人體代謝後,其代謝產物卻是有毒的。
由於細菌(原核細胞)在吸收、代謝、染色體結構和 DNA 修復過程等方面都與哺乳動物細胞不同,因此它們缺乏哺乳動物完整的代謝系統來「活化」這些化學物質。
為了解決這個問題,TG 471 試驗規定必須在有和沒有外源性代謝活化系統(exogenous metabolic activation system)的條件下進行。
最常用的代謝活化系統是S9 混合物(S9 mix)。
• S9 是從經過酶誘導劑(如 Aroclor 1254 或苯巴比妥與 β-萘黃酮的組合)處理過的齧齒動物肝臟中提取的線粒體後組分。
• S9 混合物提供了代謝酶,允許待測化學品在體外發生代謝轉化。
• 這樣一來,即使是需要肝臟活化才能致突變的物質,也能在實驗中被有效地檢測出來。
4. 試驗的實施與限制
TG 471 規範了兩種主要的測試程序:
1. 平板摻入法(Plate incorporation method):將細菌懸浮液、待測物(和 S9 混合物)與表層瓊脂混合後,立即鋪到最小培養基平板上。
2. 預孵育法(Preincubation method):先讓待測物與菌株(和 S9 混合物)預孵育 20 分鐘或更長時間後,再與表層瓊脂混合並鋪盤,。對於某些化學物質類別(例如短鏈脂肪族亞硝胺、偶氮染料、硝基化合物),預孵育法可能檢測效率更高。
劑量與判讀:
• 可溶且無細胞毒性的物質,建議最大測試濃度為 5 mg/plate 或 5μl/plate。
• 判讀結果主要基於是否存在濃度相關性的增加,或在至少一種菌株、一個或多個濃度上,有可重現的菌落數增加(無論有無代謝活化系統)。
• 一個明確的陽性結果,表明該物質會透過鹼基替換或移碼在細菌基因組中誘導點突變。
重要限制: 儘管 TG 471 試驗具有快速、廉價且易於操作的優點,在基因毒性篩選中提供了極為寶貴的數據,但它並非萬能的。
• 由於使用的是原核細胞系統,它無法完全模擬哺乳動物體內所有條件。
• 它無法提供物質在哺乳動物體內致突變或致癌潛力的直接資訊。
• 它可能不適用於某些類型的化學品,例如具有高度殺菌作用的化合物(如某些抗生素)。
• 同時,陽性結果與哺乳動物致癌性之間的相關性並非絕對,某些致癌物質可能因作用機制不同(非基因毒性或在細菌細胞中不存在的機制)而無法被此試驗檢測到。
總結來說,TG 471 細菌回復突變試驗就像是化學品進入生物體安全評估前的第一道「化學警報」。它利用經過基因改造的微小細菌,高效、準確地揪出那些可能改變我們 DNA 藍圖的潛在致病因子。
付款方式請點我
OECD 測試指南 471(Test Guideline 471),通常被視為化學品安全評估中的基石之一,其正式名稱為「細菌回復突變試驗」(Bacterial Reverse Mutation Test)。這項試驗的目標是作為一種初步篩選工具,用於快速且經濟地評估化學物質是否具有引起基因毒性(Genotoxic Activity)的潛在能力。
1. 檢測核心:危險的「點突變」
基因毒性的危害主要來自於對遺傳物質(DNA)的永久性損害。TG 471 實驗的核心在於檢測一種稱為「點突變」(Point Mutations)的特定 DNA 損傷。點突變是指 DNA 序列中,單一或少數幾個鹼基對發生替換、添加或刪除的微小變化。雖然這種變化看似微不足道,但資料指出,點突變與許多人類遺傳性疾病以及體細胞中癌基因和腫瘤抑制基因的腫瘤形成過程密切相關。
TG 471 正是透過偵測兩種主要類型的點突變來評估化學品的潛在危害:
- 鹼基替換突變(Base Substitution Mutagens):改變 DNA 中的鹼基對,。
- 移碼突變(Frameshift Mutagens):導致 DNA 中添加或刪除一個或多個鹼基對,改變了遺傳密碼的「閱讀框架」。
2. 實驗原理:讓「殘缺」的細菌起死回生。
這項試驗之所以被稱為「回復突變」(Reverse Mutation),是因為它的機制是建立在修復一個預先存在的缺陷之上。
實驗室使用的模型: TG 471 試驗使用經過特殊設計的沙門氏菌(Salmonella typhimurium)和大腸桿菌(Escherichia coli)菌株。這些菌株被稱為「營養缺陷型」,因為它們被賦予了無法合成某種生長必需氨基酸(例如組氨酸或色氨酸)的基因缺陷。
回復突變的過程:
1. 將這些殘缺的細菌懸浮液暴露於待測化學物質中。
2. 如果該化學物質具有致突變性,它會對細菌的 DNA 造成進一步的突變。
3. 如果這個新的突變剛好逆轉了(revert)原有的缺陷,那麼細菌就重新獲得了合成該必需氨基酸的能力。
4. 隨後,研究人員將混合物塗布在一個缺乏該必需氨基酸的培養基上。
5. 在兩到三天 (48 至 72 小時) 的孵育後,只有那些發生了「回復突變」、重新獲得生長能力的細菌才能形成菌落。
6. 計數這些「突變菌落」(revertant colonies)的數量,並將其與未暴露於化學物質的溶劑對照組(solvent control)的自發突變菌落數進行比較,即可判斷化學物質是否具有致突變性。
為了確保對各種致突變機制都能有效檢測,試驗必須使用至少五種菌株。例如,許多沙門氏菌菌株的突變位點是 GC 鹼基對,因此可能無法檢測某些氧化性誘變劑;因此,建議加入 AT 鹼基對突變位點的菌株,如大腸桿菌 WP2 菌株或沙門氏菌 TA102。
3. S9 混合物的必要性:模擬人體代謝
在評估化學物質毒性時,最大的挑戰之一是:許多物質本身無害,但被人體代謝後,其代謝產物卻是有毒的。
由於細菌(原核細胞)在吸收、代謝、染色體結構和 DNA 修復過程等方面都與哺乳動物細胞不同,因此它們缺乏哺乳動物完整的代謝系統來「活化」這些化學物質。
為了解決這個問題,TG 471 試驗規定必須在有和沒有外源性代謝活化系統(exogenous metabolic activation system)的條件下進行。
最常用的代謝活化系統是S9 混合物(S9 mix)。
• S9 是從經過酶誘導劑(如 Aroclor 1254 或苯巴比妥與 β-萘黃酮的組合)處理過的齧齒動物肝臟中提取的線粒體後組分。
• S9 混合物提供了代謝酶,允許待測化學品在體外發生代謝轉化。
• 這樣一來,即使是需要肝臟活化才能致突變的物質,也能在實驗中被有效地檢測出來。
4. 試驗的實施與限制
TG 471 規範了兩種主要的測試程序:
1. 平板摻入法(Plate incorporation method):將細菌懸浮液、待測物(和 S9 混合物)與表層瓊脂混合後,立即鋪到最小培養基平板上。
2. 預孵育法(Preincubation method):先讓待測物與菌株(和 S9 混合物)預孵育 20 分鐘或更長時間後,再與表層瓊脂混合並鋪盤,。對於某些化學物質類別(例如短鏈脂肪族亞硝胺、偶氮染料、硝基化合物),預孵育法可能檢測效率更高。
劑量與判讀:
• 可溶且無細胞毒性的物質,建議最大測試濃度為 5 mg/plate 或 5μl/plate。
• 判讀結果主要基於是否存在濃度相關性的增加,或在至少一種菌株、一個或多個濃度上,有可重現的菌落數增加(無論有無代謝活化系統)。
• 一個明確的陽性結果,表明該物質會透過鹼基替換或移碼在細菌基因組中誘導點突變。
重要限制: 儘管 TG 471 試驗具有快速、廉價且易於操作的優點,在基因毒性篩選中提供了極為寶貴的數據,但它並非萬能的。
• 由於使用的是原核細胞系統,它無法完全模擬哺乳動物體內所有條件。
• 它無法提供物質在哺乳動物體內致突變或致癌潛力的直接資訊。
• 它可能不適用於某些類型的化學品,例如具有高度殺菌作用的化合物(如某些抗生素)。
• 同時,陽性結果與哺乳動物致癌性之間的相關性並非絕對,某些致癌物質可能因作用機制不同(非基因毒性或在細菌細胞中不存在的機制)而無法被此試驗檢測到。
總結來說,TG 471 細菌回復突變試驗就像是化學品進入生物體安全評估前的第一道「化學警報」。它利用經過基因改造的微小細菌,高效、準確地揪出那些可能改變我們 DNA 藍圖的潛在致病因子。
- 測試方法/依循標準
OECD TG-471
- 試驗菌株
S. typhimurium TA98
S. typhimurium A100
S. typhimurium TA1535
S. typhimuriumTA1537
E.coli WP2 uvrA - 試驗目的
評估試驗物質對於沙門氏菌及大腸桿菌之致突變性,試驗物質將與特定菌株共同進行培養,若試驗物質造成菌株突變,將使菌株於培養基上大量生長成肉眼可見之菌落,透過菌落之生長情形將可推論該物質是否為可能之致癌物質。
付款方式請點我